Verhandlungstermin in Sachen VII ZR 151/18 (Haftung der “Benannten Stelle” im Zusammenhang mit dem Austausch von Silikonbrustimplantaten des französischen Herstellers PIP?) am 19. September 2019,
9.00 Uhr
 Der unter anderem für Rechtsstreitigkeiten über Schadensersatzansprüche wegen fehlerhafter Gutachten zuständige VII. Zivilsenat des Bundesgerichtshofs verhandelt im Anschluss an sein früheres Urteil vom 22. Juni 2017 (vgl. zu diesem Verfahren die Pressemitteilungen Nrn. 94/2017, 44/2017 und 52/2015) erneut über eine Schadensersatzklage, die die Frage der Haftung der sogenannten Benannten Stelle im Sinne des europäisch harmonisierten Medizinprodukterechts für die Folgen der Verwendung von Silikonbrustimplantaten des französischen Unternehmens Poly Implant Prothèse (PIP) betrifft.
Der unter anderem für Rechtsstreitigkeiten über Schadensersatzansprüche wegen fehlerhafter Gutachten zuständige VII. Zivilsenat des Bundesgerichtshofs verhandelt im Anschluss an sein früheres Urteil vom 22. Juni 2017 (vgl. zu diesem Verfahren die Pressemitteilungen Nrn. 94/2017, 44/2017 und 52/2015) erneut über eine Schadensersatzklage, die die Frage der Haftung der sogenannten Benannten Stelle im Sinne des europäisch harmonisierten Medizinprodukterechts für die Folgen der Verwendung von Silikonbrustimplantaten des französischen Unternehmens Poly Implant Prothèse (PIP) betrifft.
Sachverhalt:
Die Klägerin, eine Krankenkasse, macht geltend, sie habe die Kosten für Revisionsoperationen bei ihr gesetzlich versicherter Patientinnen getragen, denen Silikonbrustimplantate des Herstellers PIP eingesetzt worden seien. Sie nimmt aus übergegangenem Recht die Beklagte, die als Benannte Stelle im Auftrag von PIP bei dem vom Hersteller durchzuführenden EU-Konformitätsbewertungsverfahren nach Anhang II der Richtlinie 93/42/EWG mitwirkte, auf Erstattung dieser Kosten in Anspruch.
Die Beklagte führte von 1997 bis 2010 die Bewertung des Qualitätssicherungssystems und die Prüfung der Auslegungsdokumentation der PIP durch. Die Durchführung dieses Konformitätsbewertungsverfahrens berechtigte die PIP als Herstellerin von Medizinprodukten, auf von ihr richtlinienkonform gefertigten Brustimplantaten ein CE-Kennzeichen anzubringen und ist nach § 6 Abs. 1 Medizinproduktegesetz Voraussetzung dafür, dass Medizinprodukte in Deutschland in den Verkehr gebracht werden dürfen.
Die für PIP zuständige französische Aufsichtsbehörde stellte im März 2010 fest, dass dort nicht das eigentlich vorgesehene Rohmaterial für die Implantate verwendet wurde, sondern nicht für den menschlichen Körper zugelassenes Industriesilikon. Bei den Untersuchungen stellte sich heraus, dass PIP vor Kontrollen der französischen Behörden und Überprüfungen durch die Beklagte den Herstellungsprozess auf den zertifizierten Ablauf mit der Verwendung des zugelassenen Silikons umgestellt und sämtliche Hinweise auf die Verwendung von Industriesilikon versteckt hatte. PIP meldete im Jahr 2011 Insolvenz an und wurde liquidiert. Das Bundesamt für Arzneimittel und Medizinprodukte (BfArM) empfahl Anfang 2012 die Entfernung der betroffenen Silikonbrustimplantate als Vorsichtsmaßnahme.
Die Klägerin begehrt von der Beklagten die Zahlung von 50.287,15 € nebst Zinsen sowie die Feststellung der Verpflichtung der Beklagten, einen darüber hinaus gehenden künftigen Regressschaden zu ersetzen. Nach ihrem Vortrag hat sie in 26 Fällen die Operationskosten für bei ihr versicherte Frauen erstattet, denen in den Jahren 2003 bis 2010 von PIP hergestellte Silikonbrustimplantate eingesetzt worden seien und die aufgrund der Empfehlung des BfArM diese Implantate hätten entfernen lassen.
[affilinet_performance_ad size=728×90]
Bisheriger Prozessverlauf:
Die Klage ist in beiden Vorinstanzen erfolglos geblieben. Mit der vom Oberlandesgericht zugelassenen Revision verfolgt die Klägerin ihre Klageanträge weiter.
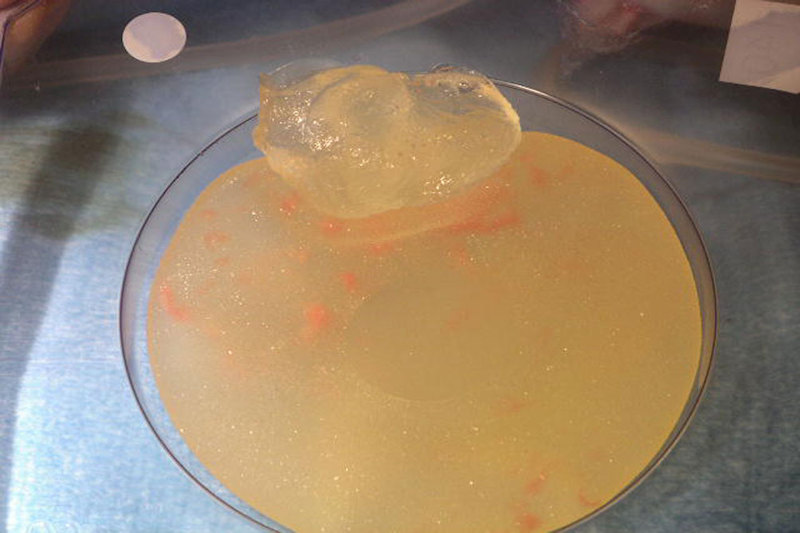
Von Gabriel J Kaufman, Rita A Sakr, Cyrille Inguenault, Isabelle Sarfati, Claude Nos and Krishna B Clough – Gabriel J Kaufman, Rita A Sakr, Cyrille Inguenault, Isabelle Sarfati, Claude Nos and Krishna B Clough: Silicone migration to the contralateral axillary lymph nodes and breast after highly cohesive silicone gel implant failure: a case report. In: Cases J 2, 2009, 420 doi:10.1186/1757-1626-2-6420 (Open Access), CC BY-SA 3.0, Link
Das Oberlandesgericht hat die Auffassung vertreten, ein Anspruch der Klägerin gegen die Beklagte komme unter keinem rechtlichen Gesichtspunkt in Betracht. Da eine Haftung der Beklagten bereits aus Rechtsgründen ausscheide, sei es unerheblich, ob der Beklagten im Zusammenhang mit der Überprüfung und Zertifizierung des Qualitätssicherungssystems und der Auslegungsdokumentation Pflichtverletzungen vorgeworfen werden könnten, denn etwaige Pflichten hätten jedenfalls nicht gegenüber den Versicherten der Klägerin bestanden.
Unmittelbare vertragliche Ansprüche zwischen den versicherten Frauen und der Beklagten – die dann nach § 116 SGB X auf die Klägerin übergegangen wären – bestünden mangels einer direkten rechtsgeschäftlichen Beziehung nicht. Ein Schadensersatzanspruch folge auch nicht aus § 280 Abs. 1 BGB in Verbindung mit den Grundsätzen des Vertrags mit Schutzwirkung zugunsten Dritter. Der zwischen PIP und der Beklagten zur Durchführung des Konformitätsbewertungsverfahrens nach § 6 Medizinproduktegesetz und der Richtlinie 93/42/EWG geschlossene Zertifizierungsvertrag entfalte keine Schutzwirkung zugunsten der versicherten Frauen, die als Patientinnen von den Brustimplantaten der PIP betroffen gewesen seien.
Ein Anspruch der Klägerin gegen die Beklagte ergebe sich ferner nicht aus § 823 Abs. 1 BGB. Der Beklagten habe bei ihrer Zertifizierungs- und Überwachungstätigkeit hinsichtlich der PIP keine besondere Garantenstellung gegenüber den Patientinnen oblegen. Ein Anspruch folge schließlich ebenso wenig aus § 823 Abs. 2 Satz 1 BGB in Verbindung mit einem Schutzgesetz. § 6 Abs. 2 Medizinproduktegesetz sei kein Schutzgesetz in diesem Sinne. Es sei nicht erkennbar, dass der deutsche Gesetzgeber einen etwaigen Verstoß gegen § 6 Abs. 2 Medizinproduktegesetz mit einer deliktsrechtlichen Haftung habe verknüpfen wollen.
Der VII. Zivilsenat hat bereits mit Urteil vom 22. Juni 2017 (VII ZR 36/14) über einen Sachverhalt entschieden, der die Haftung der Beklagten als Benannter Stelle gegenüber einer Patientin betraf, die sich auf ärztlichen Rat von PIP gefertigte Brustimplantate hatte entfernen lassen. Der Senat hat in dieser Entscheidung auf der Grundlage eines Vorabentscheidungsersuchens an den Gerichtshof der Europäischen Union und dessen daraufhin ergangenen Urteils vom 16. Februar 2017 (C-219/15; vgl. dazu auch die Pressemitteilung des Gerichtshofs der Europäischen Union Nr. 14/17 vom 16. Februar 2017) dahinstehen lassen, ob grundsätzlich eine vertragliche oder deliktische Haftung Anwendung findet. Nach den in dem betreffenden Fall revisionsrechtlich maßgeblichen Feststellungen schied eine Verantwortung der Beklagten jedenfalls mangels Pflichtverletzung aus. In der nunmehr zur Verhandlung anstehenden Sache wird wiederum inmitten stehen, ob eine – und gegebenenfalls welche – Anspruchsgrundlage für das Klagebegehren in Betracht kommt und – sofern dies der Fall ist – ob die hierfür maßgeblichen Voraussetzungen erfüllt sind.
[affilinet_performance_ad size=728×90]
Vorinstanzen:
LG Nürnberg-Fürth – Urteil vom 20. März 2014 – 11 O 7069/13 in der Fassung des Berichtigungsbeschlusses vom 16. Juli 2014
OLG Nürnberg – Urteil vom 27. Juni 2018 – 4 U 979/14
Die maßgeblichen Vorschriften lauten:
- 6 Medizinproduktegesetz
(1) Medizinprodukte, mit Ausnahme von Sonderanfertigungen, Medizinprodukten aus Eigenherstellung, Medizinprodukten gemäß § 11 Abs. 1 sowie Medizinprodukten, die zur klinischen Prüfung oder In-vitro-Diagnostika, die für Leistungsbewertungszwecke bestimmt sind, dürfen in Deutschland nur in den Verkehr gebracht oder in Betrieb genommen werden, wenn sie mit einer CE-Kennzeichnung nach Maßgabe des Absatzes 2 Satz 1 und des Absatzes 3 Satz 1 versehen sind. Über die Beschaffenheitsanforderungen hinausgehende Bestimmungen, die das Betreiben oder das Anwenden von Medizinprodukten betreffen, bleiben unberührt.
(2) Mit der CE-Kennzeichnung dürfen Medizinprodukte nur versehen werden, wenn die Grundlegenden Anforderungen nach § 7, die auf sie unter Berücksichtigung ihrer Zweckbestimmung anwendbar sind, erfüllt sind und ein für das jeweilige Medizinprodukt vorgeschriebenes Konformitätsbewertungsverfahren nach Maßgabe der Rechtsverordnung nach § 37 Abs. 1 durchgeführt worden ist. Zwischenprodukte, die vom Hersteller spezifisch als Bestandteil für Sonderanfertigungen bestimmt sind, dürfen mit der CE-Kennzeichnung versehen werden, wenn die Voraussetzungen des Satzes 1 erfüllt sind. …
- 280 BGB Schadensersatz wegen Pflichtverletzung
Verletzt der Schuldner eine Pflicht aus dem Schuldverhältnis, so kann der Gläubiger Ersatz des hierdurch entstehenden Schadens verlangen. Dies gilt nicht, wenn der Schuldner die Pflichtverletzung nicht zu vertreten hat. …
- 823 BGB Schadensersatzpflicht
(1) Wer vorsätzlich oder fahrlässig das Leben, den Körper, die Gesundheit, die Freiheit, das Eigentum oder ein sonstiges Recht eines anderen widerrechtlich verletzt, ist dem anderen zum Ersatz des daraus entstehenden Schadens verpflichtet.
(2) Die gleiche Verpflichtung trifft denjenigen, welcher gegen ein den Schutz eines anderen bezweckendes Gesetz verstößt. Ist nach dem Inhalt des Gesetzes ein Verstoß gegen dieses auch ohne Verschulden möglich, so tritt die Ersatzpflicht nur im Falle des Verschuldens ein.
- 116 SGB X Ansprüche gegen Schadensersatzpflichtige
(1) Ein auf anderen gesetzlichen Vorschriften beruhender Anspruch auf Ersatz eines Schadens geht auf den Versicherungsträger oder Träger der Sozialhilfe über, soweit dieser auf Grund des Schadensereignisses Sozialleistungen zu erbringen hat, die der Behebung eines Schadens der gleichen Art dienen und sich auf denselben Zeitraum wie der vom Schädiger zu leistende Schadensersatz beziehen. …
Karlsruhe, den 13. Juni 2019
Bundesgerichtshof
[metaslider id=20815]























+ There are no comments
Add yours